研究成果詳細
遺伝子治療用ウイルスベクターの開発
要約
本学大学院生命理工学研究科の半田宏教授? 山本法明博士課程3年らによる研究グループは? アデノ随伴ウイルス(AAV)ゲノムのヒト第19番染色体への組込みを制御する因子TRP-185を発見した.研究の内容,背景,意義,今後の展開等
本学大学院生命理工学研究科の半田宏教授? 山本法明博士課程3年らによる研究グループは? アデノ随伴ウイルス(AAV)ゲノムのヒト第19番染色体への組込みを制御する因子TRP-185を発見した.
現在? 癌などの難治疾患や遺伝子疾患は的確な治療法が無く? 遺伝子治療が究極の治療法として期待されている. しかしながら? これまでの遺伝子治療に用いられたウイルスベクターでは遺伝子を染色体の特定部位へ導入することができず? それによる副作用や有害性が大きな問題であった. ところが? それを解消できるものとしてアデノ随伴ウイルス(AAV)ベクターが脚光を浴びており? 世界規模の開発研究が展開されている. というのは? AAVは自身のゲノムDNAをヒト第19番染色体の特定部位へ組込む性質をもち? かつヒトに対して非病原性で? 安全な遺伝子治療用ベクターとして応用できるからである. AAVゲノムの組込みは? AAVのコードするRep68と呼ばれる非構造タンパク質が第19番染色体上にあるRep結合部位(RBS)にリクルートされることからはじまり? 多量体化され? そのDNAヘリカーゼ活性依存的に? Rep68はDNAをほどきながらRBS下流へ移動していき? それにともないAAVゲノムもRBSの下流領域に選択的に組込まれることで完了すると考えられている. しかしながら? その複雑な組込み過程が? 如何にして細胞性因子により制御されているかは明らかになっていなかった.
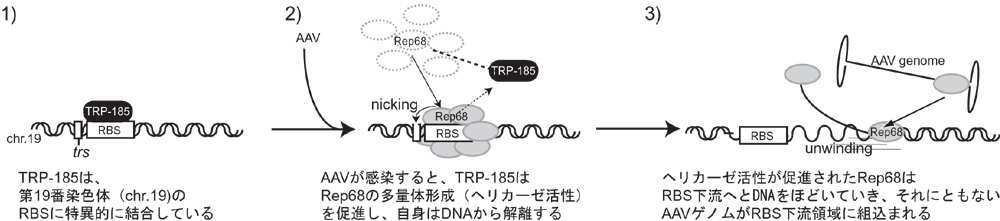
今回? 半田宏教授らのグループは? 第19番染色体上のRBS部位に特異的に結合する細胞性タンパク質TRP-185を彼らが開発したDNAアフィニティ微粒子による単離技術により発見し? この細胞性因子がRep68と一過的に結合し? Rep68の多量体化やヘリカーゼ活性を亢進することによってAAVゲノムの組込みを制御していることを突き止めた. AAVの非感染細胞ではTRP-185はRBSに選択的に結合しており(図1.1)? AAVが感染し? AAVゲノムからRep68が発現すると? TRP-185はRep68と一時的に相互作用し? RBS上でRep68の多量体化およびヘリカーゼ活性を亢進する. 面白いことに? Rep68がRBS上で多量体化するとTRP-185自身はRBSから解離するので? TRP-185は分子シャペロンとして働くと考えられる(図1.2). このTRP-185とRep68との一過性の相互作用によってAAVゲノムの組込みがRBS下流で起こる(図1.3). またTRP-185が欠落すると? その様な組込みは起こらない. 以上のことから? AAVゲノムのヒト第19番染色体のRBS下流への選択的な組込みには? 細胞性因子TRP-185が必須であることを明らかにした.
TRP-185という細胞性因子の同定によって? AAVゲノムの染色体への組込みに関する分子制御機構の一端がはじめて明らかとなった. また今回の発見は? 染色体の特異的部位への外来遺伝子を導入する制御技術の開発にも通じ? 次世代遺伝子治療用ベクターの開発へ向けて一筋の道を切り開いたものといえる.
なお? この研究成果は「Adeno-associated virus site-specific integration is regulated by TRP-185」の表題で「Journal of Virology? volume 81? issue 4」に掲載された.
図1 細胞性因子TRP-185によるAAV組込み制御モデル
| 本件に関するお問い合せ先 |
|
|---|---|
| TEL | |
| FAX | |
| URL |
*6年以上前の研究成果は検索してください